Le saviez-vous ?
En France, le parcours de soin d’un patient suspecté d’un cancer suit un protocole bien établi : imagerie (scanner, IRM, TEP-scan), biopsie, puis diagnostic et proposition de traitement. Pourtant, une étape cruciale est souvent omise ou mal appliquée : la recherche de biomarqueurs lors de la biopsie. Appelés également tests génomiques, ou analyse biomoléculaire (“biomol”), des tests permettent en effet d’identifier des mutations rares (ALK+, ROS1, RET, etc.), ouvrant la voie à des thérapies ciblées, un traitement oral sous forme de comprimés bien plus efficace et mieux toléré que le traitement par intraveineuse classique que sont la chimiothérapie et l’immunothérapie.
« La Stratégie Décennale de Lutte Contre les Cancers (2021-2030) vise à lever les inégalités d’accès aux innovations. Pourtant, des disparités persistent dans la prescription des tests. »
— Feuille de route 2026-2030, INCa (PDF à télécharger)
Or, malgré les recommandations de l’Institut National du Cancer (INCa), tous les hôpitaux ne proposent pas systématiquement ce test lors de la biopsie. En France, seulement 49,5 % des patients atteints de cancer du poumon métastatique sont testés, alors que l’INCa préconise une analyse génomique pour tous les cancers avancés.
Pourquoi une telle disparité ? Explications.
Un parcours de soin incomplet
Dès qu’un cancer est suspecté, le patient subit une série d’examens pour localiser la tumeur et évaluer son extension. Ces examens d’imagerie (scanner, IRM, puis TEP-scan) sont systématiques et remboursés à 100 %.
Si le TEP-scan révèle la présence de cellules cancéreuses, on procède à une biopsie afin de prélever un échantillon de la tumeur pour confirmer le diagnostic et analyser son profil génétique (recherche de mutations). Or, si la biopsie est toujours réalisée, l’analyse génomique (ou analyse biomoléculaire) qui suit ne l’est pas systématiquement, surtout en dehors des centres experts (Centres de Lutte Contre le Cancer, Centres Hospitaliers Universitaires, Centres labellisés CLIP²).
« Actuellement, les tests moléculaires sont principalement réalisés pour les patients présentant un cancer avancé ou métastatique. Et cela, car les traitements associés à un biomarqueur ne sont autorisés que pour ces patients.
[…] Ils sont demandés quand le médecin envisage la prescription d’un traitement conditionné par la présence d’un biomarqueur. »
— Institut National du Cancer (INCa), 2016
Ainsi, dans les faits :
- Seulement 49,5 % des patients atteints de cancer du poumon métastatique bénéficient d’un test génomique. ScienceDirect, 2019
- Les mutations rares (ROS1, RET, NTRK, HER2) sont encore moins recherchées que les mutations fréquentes (EGFR, ALK). ScienceDirect, 2025
Or sans test génomique, le médecin ne peut pas savoir si le patient est éligible à une thérapie ciblée (comme le crizotinib pour ALK/ROS1, le selpercatinib pour RET…).
Résultat : le patient se voit proposer une chimiothérapie conventionnelle, alors qu’une alternative plus efficace et mieux tolérée existe, mais n’a pas été identifiée faute de test.
« Les thérapies ciblées ont révolutionné la lutte contre le cancer. Pourtant, parce que les tests génétiques qui permettent de déterminer quels patients pourront en bénéficier sont partiellement remboursés, tous ne peuvent pas en bénéficier. »
Pourquoi les tests génomiques ne sont-ils pas systématiques ?
Les tests génomiques permettent d’identifier des mutations génétiques spécifiques dans les cellules cancéreuses, comme celles des gènes EGFR, ALK, ROS1, KRAS, NTRK, RET, HER2, MET, etc. Ces tests, apparus dans les années 2010 avec le développement de la médecine de précision, utilisent des techniques avancées comme le séquençage haut débit (NGS) ou les biopsies liquides (analyse de l’ADN tumoral dans le sang). Leur objectif : adapter le traitement à la mutation du patient, en évitant des chimiothérapies inutiles et en proposant des thérapies ciblées, bien plus efficaces et moins toxiques.
Ces tests restent onéreux en raison de leur complexité technique et de leur caractère innovant. En France, leur remboursement a été progressivement introduit à partir des années 2010-2015, mais il reste partiel et inégal :
- Les tests pour les mutations fréquentes sont rapides et peu coûteux, et remboursés à 100 % pour les cancers métastatiques, depuis les recommandations de l’INCa (Institut National du Cancer). Ce sont les tests ciblés “PCR”, “FISH”, “IHC”, “NGS” petit panel…
- Les tests pour les mutations plus rares utilisent des techniques permettant de tester des centaines de mutations à la fois : les biopsies liquides ou séquençage large (“NGS” grand panel). Ils sont coûteux et soumis à un remboursement dérogatoire et partiel (centres experts, essais cliniques).
Cette situation crée une inégalité d’accès : les patients suivis dans des centres experts (CLCC, CHU) bénéficient plus facilement de ces tests, tandis que ceux pris en charge dans des hôpitaux généraux ou en zone rurale risquent de passer à côté de solutions thérapeutiques adaptées.
« 77 % des Français estiment qu’il existe des inégalités face au cancer, et le lieu de résidence apparaît comme le principal facteur d’inégalité (38 % des répondants).
[…] Un patient sur cinq pris en charge à l’Institut Curie vient de province. »
— Baromètre de l’Institut Curie, 2026
Un combat reste donc à mener pour généraliser et démocratiser ces analyses, afin que chaque patient puisse bénéficier d’un diagnostic complet et personnalisé. Parlez-en à votre oncologue !
Comment accéder aux tests génomiques dans un CHU ?
- Demandez un test à votre oncologue : Les CHU proposent des tests génomiques pour les cancers métastatiques (ex. : NGS, FISH, PCR).
- Orientation vers un CLCC : Si votre CHU ne réalise pas le test, votre médecin peut vous orienter vers un Centre de Lutte Contre le Cancer (CLCC) partenaire.
- Essais cliniques : Les CHU labellisés CLIP² (ex. : Paris, Lyon, Toulouse) proposent des screenings moléculairesdans le cadre d’essais.
Ressources utiles
- Site de l’INCa : Liste des établissements autorisés (même si la carte est actuellement hors service, les données sont accessibles).
- Unicancer : Liste des CLCC, établissements privés spécialisés en cancérologie.
- CLIP² (Centres investigateurs spécialisés dans les essais cliniques) : Liste des CLIP² 2024-2029.pdf
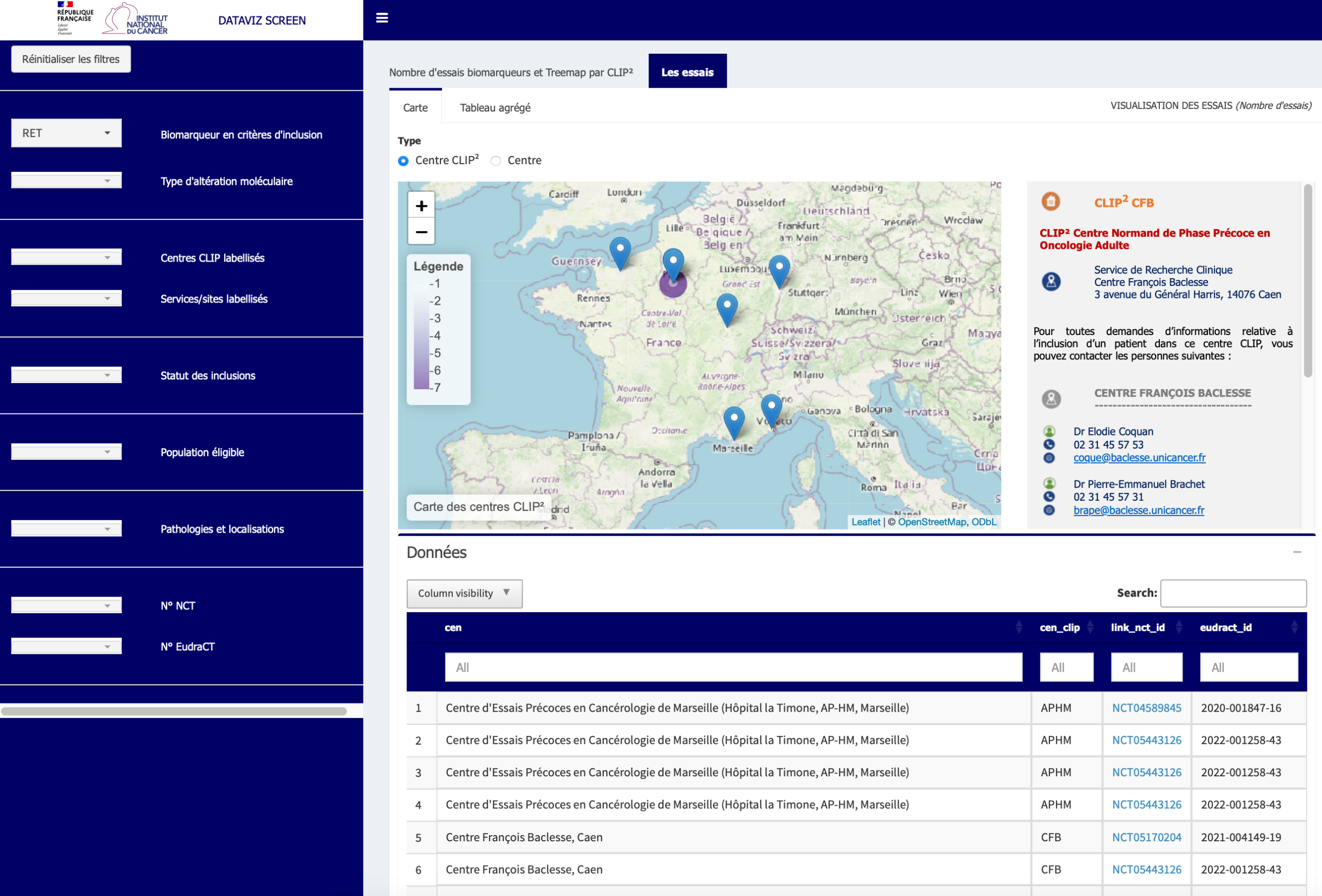
- Dataviz. En 2022, un nouvel outil interactif de datavisualisation a été mis en place pour permettre aux acteurs de la recherche clinique de consulter facilement les essais avec screening moléculaire. Il inclut un moteur de recherche pour sélectionner les essais par biomarqueur ou altération biologique, avec un lien vers ClinicalTrials.gov pour plus d’informations.
Données générales sur la santé en France
- Observatoire de la santé : une application cartographique en libre-service
- Carte interactive de la densité des professionnels de santé en France (datagouv)
- Carte des déserts médicaux en France (2025) (ici France bleu)
Article rédigé par EF le 11 mars 2026 avec l'aide de l'IA Mistral